Covid-19: Impfungen & Impfschutz
Welche Impfungen gibt es? Wie werden diese verabreicht?
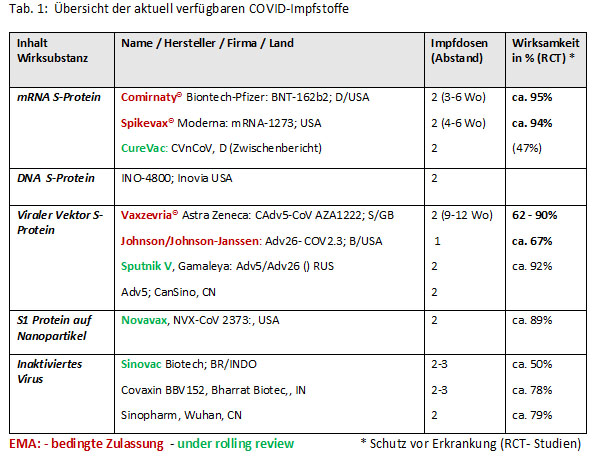
Die klinische Erprobung der ersten COVID-Impfstoffe begann am 16. März 2020 (2 ½ Monate nach der Entdeckung von SARS-CoV-2). Am 2.12.2020 (nur 8 ½ Monate später und in Rekordzeit) wurde der erste mRNA-Impfstoff (in Großbritannien) zugelassen. Derzeit stehen in Deutschland zwei mRNA-Impfstoffe und zwei Vektor-Impfstoffe zur Verfügung (siehe Tab. 1), die alle eine Immunantwort gegen das Spike-Protein auslösen. Weitere Impfstoffe sind im Zulassungsverfahren der europäischen Zulassungsbehörde (EMA).
Außer dem Vektor-Impfstoff von Janssen müssen die Impfstoffe zweimal verabreicht werden, um die volle Schutzwirkung zu erreichen. Während für die mRNA-Impfstoffe zur optimalen Schutzwirkung ein Dosisintervall von 3-6 Wochen (Comirnaty®) bzw. 4-6 Wochen (Spikevax®) empfohlen wird, nimmt die Schutzwirkung bei Vaxzevria® mit längeren Intervallen kontinuierlich zu, so dass ein Abstand von (9-) 12 Wochen günstiger ist. Sollte der empfohlene Abstand zwischen der 1. und 2. Impfstoffdosis überschritten worden sein, wird die Impfserie fortgesetzt und muss nicht neu begonnen werden. Zu beachten ist zudem, dass die Schutzwirkung jeder Impfdosis frühestens nach 10-14 Tagen eintritt.
Die Impfungen sind nach entsprechender Aufklärung und schriftlichem Einverständnis unter adäquaten Infektionsschutzmaßnahmen (Desinfektion, Handschuhe, Maske beim Impfenden und Geimpften) strikt intramuskulär zu verabreichen, auch bei antikoagulierten Patienten (dünne Kanüle, anschließende Kompression). Die Nachbeobachtungszeit beträgt mindestens 15 Minuten, bei bestimmten Risikopersonen (Anaphylaxie-Anamnese, schwere kardiopulmonale Erkrankungen) entsprechend länger. Zu anderen planbaren Impfungen soll ein Mindestabstand von 14 Tagen vor und nach jeder COVID-19-Impfstoffdosis eingehalten werden (ausgenommen Notfallimpfungen). Es besteht keine Notwendigkeit, vor Verabreichung einer COVID-19-Impfung das Vorliegen einer akuten asymptomatischen oder (unerkannt) durchgemachten SARS-CoV-2-Infektion labordiagnostisch auszuschließen.
Wie gut schützen die Impfstoffe?
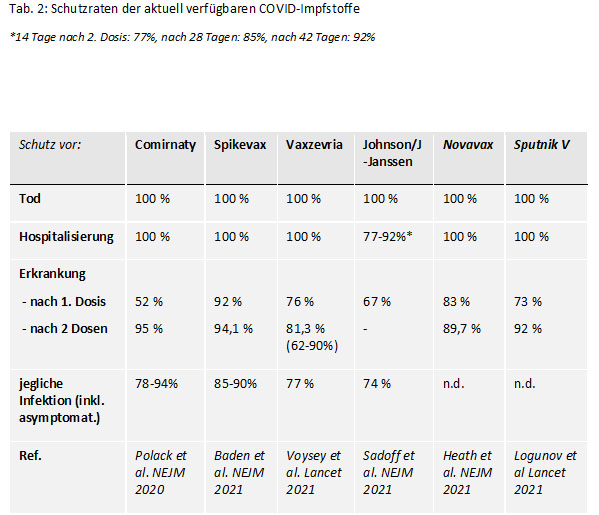
Alle zugelassenen Impfstoffe zeigten in randomisierten Placebo-kontrollierten Studien (RCT) einen sehr hohen Schutz vor schwerer oder gar tödlicher Erkrankung über alle Altersklassen (siehe Tab. 2).
Während der Schutz vor Hospitalisierung ebenfalls sehr gut ist, fällt der Schutz vor Infektion und/oder leichter Erkrankung deutlich geringer aus, so dass auch bei Geimpften mit Infektionen und der Gefahr einer Ansteckung anderer gerechnet werden muss. Die RCT-Studien (siehe Tab. 1) wurden während eines Zeitraumes durchgeführt, in dem ausschließlich oder ganz überwiegend der ursprüngliche Wuhan-Wildvirustyp zirkulierte. Die aktuell verfügbaren Impfstoffe sind auch gegen die Alpha-Virusvariante gut wirksam, gegen die Beta-Variante schützen jedoch nur die mRNA-Impfstoffe. Der Impfschutz gegen Infektionen durch die Delta-Variante ist bei allen Impfstoffen geringer und erst nach der 2. Dosis in einem zufriedenstellenden Bereich. Der Impfschutz vor schweren Verläufen und Hospitalisierung durch Infektionen mit dem Deltavirus ist jedoch bei allen Impfstoffen hoch (> 90%).
Der Impfschutz kann bei Immunsuppression deutlich geringer ausfallen. Dies gilt vor allem für Patienten nach Transplantation solider Organe und Patienten mit immunschwächender (B-Zell-depletierender) Therapie (z. B. Rituximab). Eine aktuelle Auswertung aus Israel zu Impfdurchbrüchen nach mRNA-Impfung ergab, dass bei ca. 5,4 Millionen Geimpften 397 vollständig geimpfte Patienten im Alter von durchschnittlich 71 Jahren wegen einer COVID-Erkrankung stationär aufgenommen werden mussten. Bei 96 % dieser Patienten lagen Grunderkrankungen mit erhöhtem Risiko vor, bei 40 % bestand eine Immunsuppression, 22 % der Patienten verstarben. Bei Immunsupprimierten sind daher serologische Kontrollen (anti-Spikeprotein-ELISA, Neutralisationstest bzw. Neutralisations-Surrogat-Test) zur Überprüfung des Impferfolgs empfehlenswert, die frühestens 4 Wochen nach der letzten Impfung erfolgen sollten. Bei fehlender oder mangelhafter Immunantwort ist die Gabe einer oder ggf. mehrerer weiterer Impfstoffdosen angezeigt.
Welche Impf-Nebenwirkungen können auftreten?
Lokale und systemische Nebenwirkungen (Kopf/Gliederschmerzen, Abgeschlagenheit, Fieber, Schüttelfrost) sind nach allen verfügbaren COVID-Impfstoffen häufig und klingen meist innerhalb weniger Tage wieder ab. Allergische Reaktionen (Exantheme u.a.) treten häufiger bei mRNA-Impfstoffen auf und können sich mit einer Inzidenz von 1: 40.-200.000 als Anaphylaxie (Herzrasen, niedriger Blutdruck, Atemnot, Schwellungen an Haut, Zunge oder Kehlkopf/Glottisödem) manifestieren, die meist innerhalb von 30 Minuten nach Impfung auftritt und i.d.R. gut auf eine entsprechende Therapie (Adrenalin, Volumengabe, Antihistaminika, Glukokortikoide, Salbutamol) anspricht. Sehr selten wurden auch neurologische Nebenwirkungen wie Gesichtsnerv-Lähmung (Facialis-Paresen), Taubheitsgefühl, oder ein Guillain-Barré-Syndrom berichtet, bei denen ein kausaler Zusammenhang nicht ausgeschlossen werden kann.
Nach der Gabe von Vektor-Impfstoffen wurde vor allem bei jüngeren Frauen eine starke Verminderung der Blutplättchen (Thrombozyten = Thrombopenie)mit ungewöhnlichen venösen und arteriellen Thromben (zerebrale Sinusvenen, Thromboembolien im Splanchicusgebiet) beobachtet, welche als TTS (unusual thrombosis with thrombocytopenia syndrome) bezeichnet wurde. Mittlerweile sind mehrere hundert Fälle mit einer Letalität von 10-20 % dokumentiert, die meist 4-16 Tage nach der Erstimpfung aufgetreten waren. Bei der Mehrzahl der Fälle waren Antikörper gegen Plättchen-Faktor 4 nachweisbar, wie sie auch bei Heparin-induzierter Thrombopenie vom Typ 2 (HIT-2) auftreten. Die ständige Impfkommission (STIKO) empfiehlt Vektorimpfstoffe daher nur noch für Personen ab einem Alter von 60 Jahren. Zudem wurde nach Vektor-Impfstoffen sehr selten ein Kapillarlecksyndrom (CLS) beobachtet. Da in einigen dieser Fälle anamnestisch ein CLS bekannt war, sind Vektor-Impfstoffe bei solchen Personen kontraindiziert.
Nach der Gabe von mRNA-Impfstoffen kommt es mit einer Inzidenz von 1-3 Fällen pro 1 Million Impfungen zu einer Myo- und/oder Perikarditis. Diese manifestierte sich meist 2-14 Tage nach der 2. Impfdosis und betrifft bevorzugt junge männliche (76 %) Erwachsene und Heranwachsende (Altersmedian: 26 Jahre). Verdächtige Symptome sind Herzrhythmusstörungen (Palpitationen, Herzjagen, Herzstolpern), Atemnot und/oder Thoraxschmerzen. Der Verlauf ist meist gutartig und ohne Spätfolgen. Vereinzelt berichtete Todesfälle betrafen in erster Linie ältere und vorerkrankte Patienten.
Impfungen für Kinder und Schwangere?
Die mRNA-Impfstoffe sind zugelassen für Kinder und Jugendliche ab dem 12. Lebensjahr sowie eingeschränkt (nur nach sorgfältiger Nutzen-/Risiko-Abwägung) auch für Schwangere und Stillende. Die Vektor-Impfstoffe sind nur für Erwachsene ab dem 18. Lebensjahr zugelassen. Nachdem mittlerweile umfangreichere Daten zur Sicherheit und Wirksamkeit bei Kindern und Jugendlichen vorliegen, empfiehlt die STIKO die Impfung mit mRNA-Impfstoffen auch für Kinder ab dem 12. Lebensjahr. Besonders indiziert ist die Impfung für Kinder mit Grunderkrankungen, die ein erhöhtes Risiko für schwere COVID-Verläufe darstellen.
Im Gegensatz zu einigen Fachgesellschaften gibt die STIKO derzeit keine generelle Impfempfehlung für Schwangere und Stillende. Die STIKO weist darauf hin, dass bei Vorerkrankungen und einem daraus resultierenden hohen Risiko für eine schwere COVID-19-Erkrankung oder mit einem erhöhten Expositionsrisiko aufgrund ihrer Lebensumstände nach Nutzen-Risiko-Abwägung und Aufklärung eine Impfung mit einem mRNA-Impfstoff ab dem 2. Trimenon angeboten werden kann.
Impfungen nach durchgemachter Infektion?
Aufgrund der Immunität nach durchgemachter SARS-CoV-2-Infektion sollten immungesunde Personen, die eine PCR-gesicherte SARS-CoV-2- Infektion durchgemacht haben, unabhängig vom Alter zunächst nur eine Impfstoffdosis erhalten, da sich durch eine einmalige Impfung bereits hohe Antikörperkonzentrationen erzielen lassen, die durch eine 2. Dosis nicht weiter gesteigert werden. Dies gilt auch, wenn der Infektionszeitpunkt länger zurückliegt. In der Regel erfolgt die Impfung ca. 6 Monate nach Infektion bzw. Erkrankung, kann aber bereits ab 4 Wochen nach Abklingen der COVID-Symptome bzw. nach asymptomatischer Infektion erfolgen, wenn z. B. eine Exposition gegenüber neu aufgetretenen Virusvarianten anzunehmen ist, gegen die eine durchgemachte SARS-CoV-2- Infektion allein keinen längerfristigen Schutz mehr vermittelt (immune escape-Varianten). Ob und wann später eine 2. COVID-19-Impfung notwendig ist, lässt sich gegenwärtig nicht sagen. Bei Personen mit Immundefizienz sollte jedoch im Einzelfall und abhängig von Art und Ausprägung der Immundefizienz entschieden werden, ob eine einmalige Impfstoffdosis ausreicht oder eine vollständige Impfserie verabreicht werden sollte (ggf. Antikörper-Bestimmung im Verlauf).
Wie geht es weiter mit den Impfungen?
Aufgrund der Empfehlung, Vektor-Impfstoffe nur noch bei Personen im Alter ? 60 Jahren anzuwenden, empfiehlt die STIKO bei < 60-Jährigen, die Vaxzevria® als 1. Impfdosis erhalten hatten, ein heterologes Impfschema, d. h. die 2. Impfung mit einem mRNA- Impfstoff in einem Abstand von mindestens 4 Wochen durchzuführen. Diese Empfehlung wurde nun auch auf > 60-Jährige erweitert, da mehrere Studien zeigten, dass die Antikörper- wie die die T-Zell-basierte Immunantwort nach diesem heterologen Impfschema signifikant besser ist als nach zweimaliger Vaxzevria®-Impfung, so dass ein besserer Schutz auch gegen die Delta-Variante angenommen wird. Zudem kann eine vollständige Immunisierung in einem kürzeren Zeitrahmen erreicht werden (schon ab 4 gegenüber 9-12 Wochen).
Die bisherigen Verlaufsuntersuchungen deuten darauf hin, dass der Impfschutz nach vollständiger Immunisierung auch bei Immunkompetenten zum Teil nur über einen begrenzten Zeitraum anhält und eine Auffrischimpfung (3. Impfung) nach 6-12 Monaten sinnvoll sein kann. Einige Länder bieten daher Geimpften bereits eine dritte Impfung an (Israel ab dem 30. Lebensjahr, Frankreich ab dem 65. Lebensjahr). Zudem wird in diesen Ländern auch eine 2. Impfung empfohlen für einmalig mit dem Janssen/Johnson-Vektorimpfstoff Geimpfte sowie für Genesene, die bisher nur einmal geimpft wurden. Derzeit wird untersucht, inwieweit Antikörperbestimmungen helfen können, Indikation und Zeitpunkt solcher Auffrischimpfungen zu bestimmen. Da die Schutzwirkung der aktuell zugelassenen Impfstoffe gegen Virusvarianten wie die mittlerweile in vielen Ländern dominierende Deltavariante weniger zuverlässig wirken, werden bereits angepasste Impfstoffe klinisch getestet, welche die Mutationen der Varianten berücksichtigen.



